Gefälschte Medikamente
Re-Importe bescheren höhere Gewinne, aber sind sie auch sicher?
Gerade hatte ich ein sehr interessantes Telefongespräch mit dem Kundenservice von Boehringer Ingelheim. Es ging um das Präparat Buscopan plus.
Aufgrund der etwas ungewöhnlichen Verpackung (siehe Fotos) und meinem persönlichen Eindruck, dass die Wirkung nicht identisch ist, mit den Buscopan Tabletten, die ich davor eingenommen hatte, fragte ich direkt bei Boehringer Ingelheim nach. So erfuhr ich, dass es von unserer Bundesregierung und von den Krankenkassen gewollt ist, dass Medikamente für den deutschen Markt durch Re-Importe günstiger eingekauft werden. Im Falle von Buscopan spielt die Krankenkasse keine Rolle, weil das Präparat von den gesetzlichen Krankenkassen nicht bezahlt wird. Hier geht es rein um den Profit der Apotheken.

Buscopan – man denkt doch, dass das direkt von Boehringer Ingelheim kommt, oder? Kommt es nicht. Siehe Foto unten
Einen Re-Import erkennt man daran, dass auf der Pillenverpackung ein Aufkleber einer Arzneimittelfirma ist. In diesem Fall hier ist es die EMRAmed Arzneimittel GmbH in Trittau. Seltsam kommt mir allerdings auch vor, dass die Alufolie und die darüberliegende weiße Plastikfolie versetzt aufgebracht sind. Das kann natürlich einfach nur durch eine kleine Verschiebung bei der Produktion entstanden sein und muss nichts weiter bedeuten.
Boehringer Ingelheim versicherte mir, dass derart günstige Präparate normalerweise nicht gefälscht werden, weil man damit nicht so viel verdienen kann. Man hat mich dennoch gebeten, dass ich in die Apotheke meines Vertrauens gehe, um dort die Sache überprüfen zu lassen. Die Apotheke nimmt mit dem Hersteller Kontakt auf und sendet das Medikament ein. Da ich das Buscopan in einer anderen Stadt gekauft habe, kann ich einigermaßen sicher sein, dass hier kein Interessenskonflikt auftritt.
Auf meine Frage, weshalb Boehringer ins Ausland günstiger liefert und diese Konditionen nicht auch deutschen Apotheken anbietet, sagte man mir, dass man ein deutsches Unternehmen mit Sitz in Deutschland sei, das hier Löhne, Gehälter und Steuern zahlt, die verdient werden müssten. Auf meine Frage, ob man das Medikament nur in Deutschland produziere, bekam ich die Antwort, dass die Produktion über die ganze Welt verteilt sei.

Buscopan von Boehringer Ingelheim wurde in Frankreich hergestellt, dann umverpackt. Wer hat da die Kontrolle?
Dieses Buscopan wurde von Delpharrm Reims, Frankreich hergestellt und von MPA Pharma GmbH umverpackt. Als Pharmazeutischer Unternehmer wird EMRAmed. Arzneimittel GmbH in Trittau genannt.
Hierzu Auszüge aus der Pressemitteilung der Deutschen Pharmazeutischen Gesellschaft e.V. vom 09. Oktober 2013:
Gefälschte Arzneimittel – Gesundheitsrisiken für Patienten
Heute werden aus Kostengründen etwa 80 Prozent aller Arzneistoffe in China und Indien produziert. Wahrscheinlich treibt der Druck, immer günstiger produzieren zu müssen, die Hersteller dazu, nicht nur die Herstellung von Wirkstoffen, sondern auch die Fertigung von Zwischenprodukten und mittlerweile sogar die gesamte Produktion in fremde Länder auszulagern. In Asien hergestellt, in Ungarn oder Rumänien verpackt, in Malta kontrolliert, zum Schluss nach Deutschland transportiert: Solche „Reiserouten“ sind für Arzneimittel längst keine Ausnahme mehr. Wie viele Arzneimittel vollständig oder in Teilen im Ausland hergestellt werden, lässt sich nur schätzen, denn pharmazeutische Unternehmen sind nicht dazu verpflichtet, die Ursprungsländer und Produktionswege ihrer Medikamente anzugeben. Zwar müssen die Hersteller im Ausland die gleichen Qualitätsanforderungen erfüllen wie die hier ansässigen Unternehmen, doch wird es im Zeitalter der Globalisierung zunehmend schwieriger, die Hersteller im Ausland wirksam zu kontrollieren.
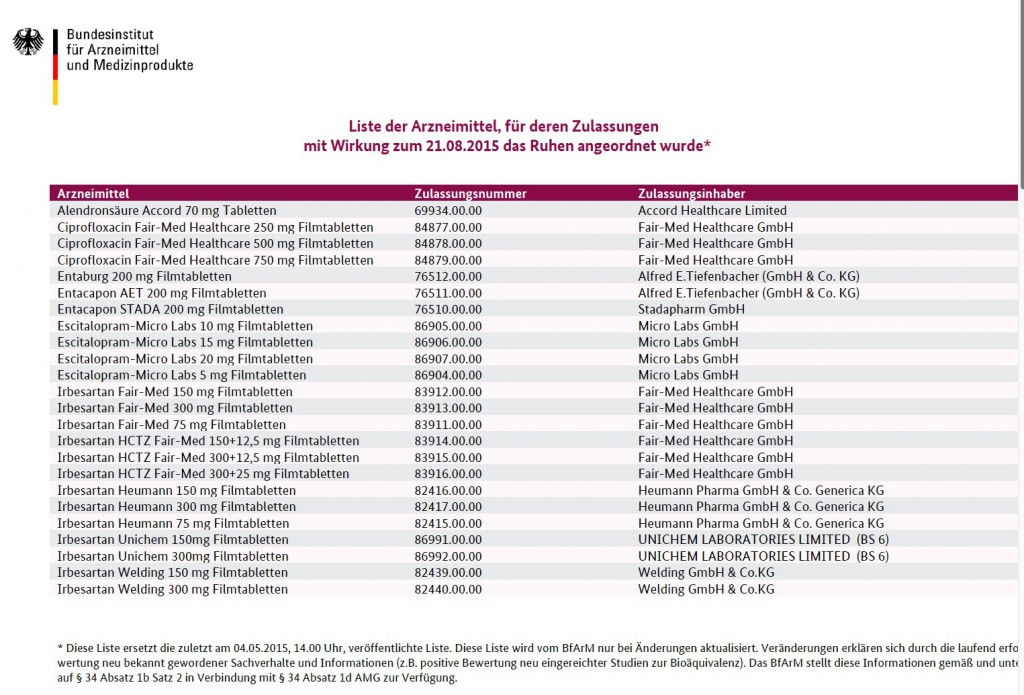
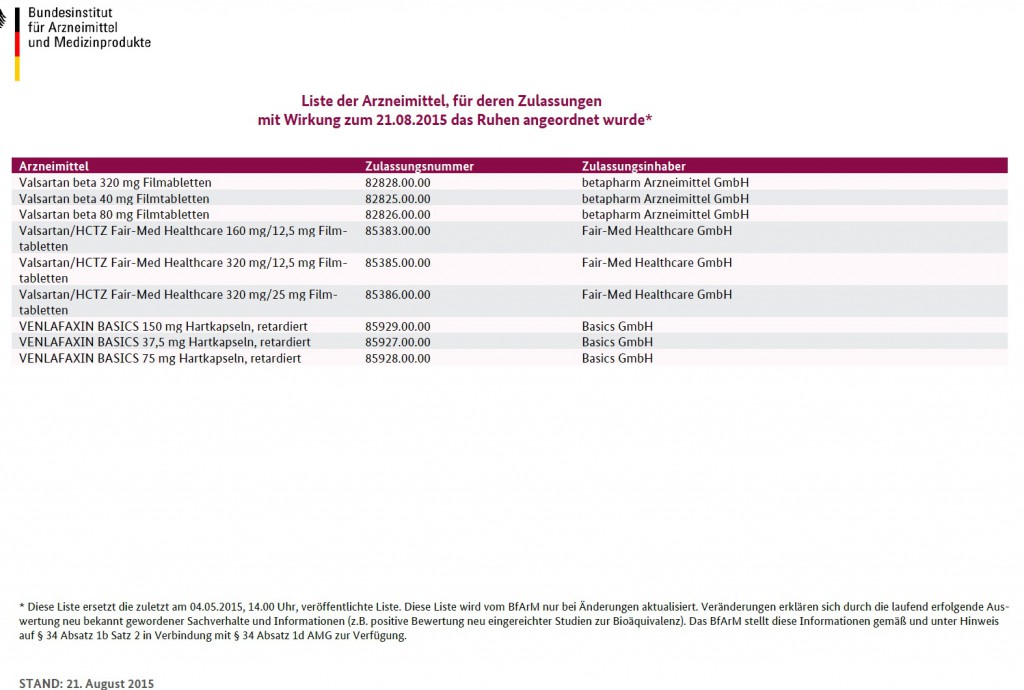
Laut dem EU-Zollbericht 2012 stehen gefälschte Arzneimittel mit knapp 24 Prozent an der Spitze gefälschter Waren, die an den Grenzen der EU entdeckt wurden. „Im illegalen Internethandel ist sogar jedes zweite Präparat gefälscht“, sagte Professor Dr. Ulrike Holzgrabe vom Institut für Pharmazeutische Chemie der Universität Würzburg. Lifestyle-Medikamente gegen Impotenz oder Haarausfall stehen ganz oben auf der Liste der am häufigsten gefälschten Medikamente. Doch längst betreffen Arzneimittelfälschungen auch „gewöhnliche“ Wirkstoffgruppen, z.B. Antibiotika, Schmerzmittel, Medikamente gegen Bluthochdruck, Medikamente gegen erhöhte Cholesterinwerte oder Verhütungsmittel wie die „Pille“.
Können sich Patienten vor Arzneimittelfälschungen schützen? Wer auf Nummer sicher gehen will, kauft Arzneimittel in der Apotheke vor Ort, denn in der „legalen“ Vertriebskette „Hersteller – Großhandel – Apotheke“ kommen Arzneimittelfälschungen so gut wie nicht vor. In Deutschland sind zwischen 1996 und 2008 nur 40 Fälle von Fälschungen im „legalen“ Vertrieb aufgetreten. Dagegen wurden schon im ersten Halbjahr 2013 vom Zoll insgesamt 1,4 Millionen gefälschte Arzneimittelpackungen sichergestellt, im Vergleich zu 2012 eine Steigerung um 15 Prozent.
Um den legalen Vertriebsweg auch künftig vor Fälschungen zu schützen, hat die EU im Juli 2011 eine Richtlinie zur Bekämpfung von Arzneimittelfälschungen veröffentlicht. In Deutschland wird dazu seit Anfang 2013 ein nationales System getestet, um die Echtheit von Arzneimitteln sicherzustellen. Arzneimittel tragen zu diesem Zweck Sicherheitsmerkmale, zum Beispiel 2D-Barcodes, mit denen der Apotheker bei der Abgabe prüfen kann, ob die Arzneimittelpackung aus legalen Quellen stammt. Wer, was in Deutschland erlaubt ist, Arzneimittel aus einer zugelassenen Versandapotheke über das Internet bestellt, sollte wachsam sein und ein gesundes Misstrauen haben, um nicht auf einen Betrüger hereinzufallen, der die Internetseite einer deutschen Versandapotheke täuschend ähnlich nachgebaut hat. Wenn Medikamente marktschreierisch angepriesen werden, wenn mit Billigstpreisen geworben wird, wenn man kein Rezept mitschicken muss, dann nichts wie Hände weg von solchen Angeboten!
Das sagt die DPhG über sich selbst:Die Deutsche Pharmazeutische Gesellschaft e.V. (DPhG) zählt mit über 10.000 Mitgliedern zu den großen wissenschaftlichen Gesellschaften in Deutschland. Die DPhG veranstaltet jährlich etwa 150wissenschaftliche Vorträge für Apotheker, ist Herausgeberin der Zeitschrift „Pharmakon“ und fördert als unabhängige Gesellschaft die wissenschaftlichen Interessen der deutschen Pharmazie.
Bei dieser Pressekonferenz wurde u. a. von Medizinerinnen angemerkt, dass Fälschungen auch über Apotheken verkauft werden, da es keinen hundertprozentigen Schutz gäbe. Oft sei es sehr schwer Fälschungen von echten Medikamenten zu unterscheiden. Nur wenn Zweifel aufkämen, würde eine Überprüfung stattfinden.
Ich habe auch in deutschen Apotheken die Erfahrung gemacht, dass rezeptpflichtige Medikamente von Apotheken-Helferinnen – sogar in Ausbildung – ausgehändigt wurden.
Am Ende trägt das Risiko immer der Patient oder die Patientin. Man sollte deshalb schon genau hinschauen, wenn das gewohnte Medikament sich in Form und Verpackung verändert hat. Und schauen Sie auch genau hin, ob es sich um einen Re-Import handelt. Fragen Sie Ihren Apotheker oder Ihre Apothekerin, weshalb sie Ihnen einen Re-Import zum gleichen Preis eines in Deutschland direkt ausgelieferten Medikaments verkauft. Manche Apotheken reagieren darauf sehr ungehalten. Das sollte man allerdings nicht einfach so hinnehmen, geht es doch um die eigene Gesundheit.
Für die immer älter werdende Gesellschaft entstehen hier neue Probleme. Ältere Menschen sind oft darauf angewiesen, dass sie ihrem Apotheker oder ihrer Apothekerin vertrauen können.

Der Aufkleber zeigt, dass es sich hier um einen Re-Import handelt