Die Hemmung der Genaktivität in Mitochondrien von Mäusen stoppt das Wachstum von Krebszellen
Ein neu entwickelter Wirkstoff hungert Krebszellen aus, indem er das Ablesen der genetischen Information der Mitochondrien verhindert. Wissenschaftler und Wissenschaftlerinnen des Max-Planck-Instituts für Biologie des Alterns, des Stockholmer Karolinska Instituts und der Universität Göteborg berichten in einer Studie, dass die chemische Verbindung auch Potential für die Krebstherapie bei Menschen haben könnte.
Mitochondrien versorgen unsere Zellen mit Energie und Bausteinen, die für die normale Funktion von Geweben und Organen unerlässlich sind. Lange Zeit ging man allerdings davon aus, dass das Wachstum von Krebszellen weniger stark vom Beitrag der Mitochondrien abhängt. Diese seit langem bestehende Lehrmeinung wurde jedoch in den letzten Jahren zunehmend in Frage gestellt. Besonders Krebsstammzellen sind in hohem Maße vom mitochondrialen Stoffwechsel abhängig. Aufgrund der zentralen Rolle der Mitochondrien für die normale Gewebefunktion und weil Medikamente, die auf die Mitochondrienfunktionen abzielen, normalerweise sehr toxisch sind, hat es sich bisher als schwierig erwiesen, Mitochondrien im Rahmen der Krebsbehandlung gezielt anzugreifen.
Jetzt hat ein internationales Forscherteam einen Weg gefunden, diese Schwierigkeiten zu überwinden. „Es ist uns gelungen, ein potenzielles Krebsmedikament zu entwickeln, das auf die Funktion der Mitochondrien abzielt, ohne schwere Nebenwirkungen zu verursachen und ohne gesunde Zellen zu schädigen“, erklärt Nina Bonekamp, eine der Hauptautorinnen der Studie. Mitochondrien enthalten ihr eigenes genetisches Material, die mitochondrialen DNA-Moleküle (mtDNA). Das Ablesen dieser Gene wird durch einen speziellen Satz von Proteinen gesteuert. Eines dieser Proteine ist das Enzym „mitochondriale RNA-Polymerase“, abgekürzt POLRMT. „Unsere früheren Studien haben gezeigt, dass sich schnell vermehrende Zellen, wie z.B. embryonale Zellen, sehr empfindlich auf eine Hemmung der mtDNA-Expression reagieren, während differenzierte Gewebe wie Skelettmuskel diesen Zustand überraschend lange tolerieren können. Wir kamen zu dem Schluss, dass POLRMT als ein Schlüsselregulator der mtDNA-Expression ein vielversprechendes Ziel darstellen könnte“, sagt Nils-Göran Larsson, Leiter des Forschungsteams.
Wirkstoff hemmt mitochondriale RNA-Polymerase
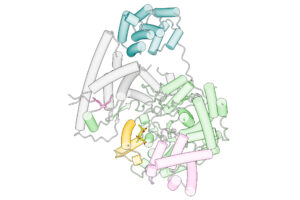
In Zusammenarbeit mit dem Lead Discovery Center, einer von Max-Planck-Innovation gegründeten Einrichtung für translationale Wirkstoffforschung, entwickelte das Forschungsteam eine Hochdurchsatz-Testmethode zur Identifikation eines POLRMT-hemmenden Wirkstoffs. Der POLRMT-Hemmer verringerte die Lebensfähigkeit von Krebszellen stark und verlangsamte das Tumorwachstum in tumortragenden Mäusen signifikant. Gleichzeitig wurde der Wirkstoff aber gut von den Tieren vertragen. „Unsere Daten deuten darauf hin, dass wir Krebszellen im Grunde aushungern und so zum Sterben bringen. Das gelingt, zumindest für eine gewisse Zeit, ohne starke Nebenwirkungen. Dies gibt uns ein potenzielles therapeutisches Zeitfenster für die Behandlung von Krebs“, sagt Nina Bonekamp. „Ein weiterer Vorteil unseres Hemmstoffs ist, dass wir genau wissen, wo er an POLRMT bindet und was er mit dem Protein macht. Das steht im Gegensatz zu einigen anderen Medikamenten, die sich sogar im klinischen Einsatz befinden“. Mit Hilfe der ACUS-Laboratorien in Köln und des Max-Planck-Instituts für biophysikalische Chemie in Göttingen identifizierte das Team die chemische Bindungsstelle des Inhibitors und erhielt Informationen über die Struktur des Komplexes aus POLRMT und Inhibitor.
Bonekamp und Larsson sind sich einig, dass es ein spannendes Unterfangen war, grundlegende Erkenntnisse in ein potenzielles Medikament umzusetzen. Umso mehr freuen sie sich über die Möglichkeiten, die ihre Erkenntnisse eröffnen werden. „Angesichts der zentralen Rolle des mitochondrialen Stoffwechsels innerhalb der Zelle bin ich sicher, dass unser Inhibitor als Werkzeug in einer Vielzahl von Bereichen Verwendung finden wird“, erklärt Nina Bonekamp. „Natürlich ist es faszinierend, sein Potenzial als Krebsmedikament weiterzuverfolgen, aber auch als Modellverbindung, um die zellulären Auswirkungen mitochondrialer Funktionsstörungen und mitochondrialer Erkrankungen besser zu verstehen.“