Das Mikrobiom als Ansatzpunkt für Therapien gegen das Altern

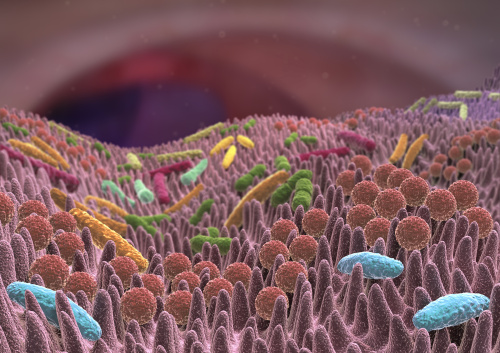
(01.09.2020) Der Darm mit seinen zahlreichen Mikroorganismen leistet einen maßgeblichen Beitrag zu unserer Gesundheit und unserem Wohlbefinden. Doch wie verändert sich das Mikrobiom des Darms – immerhin größtes Organ des menschlichen Körpers – bei hochaltrigen Menschen? Und welchen Einfluss hat seine veränderte Zusammensetzung auf die Gesundheit geriatrischer Patienten – und ihr Altern? Mit dieser Thematik setzt sich Professor Christoph Kaleta (Foto), Leiter der Arbeitsgruppe „Medizinische Systembiologie“ am Institut für Experimentelle Medizin der Christian-Albrechts-Universität zu Kiel, auseinander. In seiner Keynote „Elucidating the contribution of the gut microbiome to aging“ im Rahmen der am Donnerstag beginnenden geriatrisch-gerontologischen Online-Konferenz beleuchtet er das Thema ganzheitlich. Dabei zeigt Kaleta auf, wie mikrobiombasierte Therapien das Altern verlangsamen können. Die Online-Konferenz findet vom 3. bis 5. September statt und wird organisiert von der Deutschen Gesellschaft für Geriatrie (DGG) mit Beteiligung der Deutschen Gesellschaft für Gerontologie und Geriatrie (DGGG).
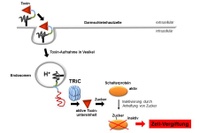
„Wir haben festgestellt, dass sich das Mikrobiom im alternden Körper opportunistisch verhält. Das bedeutet im Detail, dass es die Produktion von – für seinen Wirt vorteilhaften – Metaboliten reduziert und gleichzeitig seinen eigenen Verbrauch von Nährstoffen erhöht“, sagt Christoph Kaleta und fährt fort: „Diese verminderte Kapazität der Mikrobiota in unserem Darm spielt eine zentrale Rolle für das Altern. Erkennbar wird das beispielsweise bei der Zellproliferation und Reparatur von DNA-Schäden.“ Den Teilnehmern der Online-Konferenz wird er aufzeigen, was diese Veränderung des Mikrobioms im Detail bedeutet, aber auch, wie die Medizin es nutzen kann, um dem Altern entgegenzuwirken.
Mit der medizinischen Systembiologie Krankheiten entschlüsseln
Am Institut für Experimentelle Medizin der Universität Kiel gehen Christoph Kaleta und sein Team der Frage nach, wie unser biologisches System als Ganzes funktioniert, welche Mechanismen Krankheiten auslösen und wie das Mikrobiom mit dem Wirt interagiert. In der sogenannten Systembiologie, einer zukunftsweisenden Forschungsdisziplin, werden integrative Analysen großer Datenmengen, Modellierungen und Nasslaborexperimente vollzogen, um schlussendlich besser zu verstehen, wie biologische Prozesse ablaufen und Krankheiten entstehen. Dadurch werden einerseits Risikofaktoren identifiziert und Forscher können andererseits wesentlich besser verstehen, wie es Krankheitserregern gelingt, sich im Körper zu verbreiten. Zudem wird erkannt, wie sich diese Erreger während einer Infektion an die sich schnell verändernden Bedingungen anpassen.
Das Mikrobiom als Ansatzpunkt für Therapien gegen das Altern
Für Christoph Kaleta steht fest, dass therapeutische Interventionen, die auf das Mikrobiom ausgerichtet sind, das Altern aktiv verlangsamen können. Hierfür haben er und sein Team bereits erste Experimente mit einigen Medikamenten durchgeführt. „Beispielsweise spielt es eine wesentliche Rolle im Wirkungsmechanismus des Typ-2-Diabetes-Medikaments Metformin. Dieses ist in der Lage, die Lebensspanne in einer Vielzahl von Organismen und möglicherweise auch im Menschen zu verlängern“, so der Forscher. Experimente mit Fadenwürmern und Studien mit hochbetagten Patienten haben gezeigt, dass nach der Einnahme des Medikamentes das Mikrobiom aktiver ist.
Erfolgsversprechen Therapien: Erhöhte Kapazitäten des Mikrobioms nutzen
Die Experimente mit Metformin sind nur ein erster Nachweis dafür, dass die Erforschung biologischer Mechanismen Alterserscheinungen verbessern oder gar reduzieren kann. „Das Mikrobiom, besonders im Darm, wird zunehmend als Modulator für die Gesundheit seines Wirts anerkannt, vor allem im Kontext des Alterns“, so Christoph Kaleta. In seiner Keynote will er noch detaillierter aufzeigen, wie erfolgsversprechend Therapien sind, die direkt die Mikrobiota ansprechen. „Wenn wir die mikrobiellen Gemeinschaften im menschlichen Körper verstehen, können wir auch die Pathomechanismen menschlicher Krankheiten besser verstehen – und das Mikrobiom nutzen, um sie zu behandeln.“ Die Erkenntnisse aus der Systembiologie können auch die Therapie von Alterserscheinungen entscheidend verändern.
Zur Person:
Prof. Dr. Christoph Kaleta ist Leiter der Arbeitsgruppe „Medizinische Systembiologie“ am Institut für Experimentelle Medizin der Christian-Albrechts-Universität zu Kiel. Schwerpunkte der Forschung der Arbeitsgruppe „Medizinische Systembiologie“ sind die Aufklärung gemeinsamer Mechanismen, die menschlichen Krankheiten – besonders im Alter – zugrunde liegen sowie die Entwicklung von Modellierungsansätzen, die es ermöglichen, metabolische Interaktionen innerhalb mikrobieller Gemeinschaften sowie mit dem Wirt zu untersuchen. Unter der Leitung von Christoph Kaleta hat die Arbeitsgruppe zahlreiche Publikationen zur Funktion und dem Einfluss von Mikrobiomen bei zahlreichen Krankheiten veröffentlicht. Kaleta ist zudem Mitglied des Exzellenzclusters „Präzisionsmedizin für chronische Entzündungserkrankungen/Precision Medicine in Chronic Inflammation“ (PMI) und des Sonderforschungsbereichs „Entstehen und Funktionieren von Metaorganismen“ der Deutschen Forschungsgemeinschaft (DFG).
Termin:
Prof. Dr. Christoph Kaleta
Keynote Lecture: Elucidating the contribution of the gut microbiome to aging
Geriatrisch-gerontologische Online-Konferenz
Deutsche Gesellschaft für Geriatrie (DGG) mit Beteiligung der Deutschen Gesellschaft für Gerontologie und Geriatrie (DGGG)
Donnerstag, 3. September 2020
15:45 bis 16:25 Uhr